§ 来源:中国知网
§ 作者:朱福余 林振华 孙立魁 车国喜 屈秋锦 刘香东 刘增祥 刘成虎△
(山东省医疗器械和药品包装检验研究院 国家药品监督管理局生物材料器械安全性评价重点实验室 山东 济南 250101)
§
【摘要】
目的:建立植入了骨修复材料小型猪腰椎椎体骨组织标本的不脱钙病理组织切片制备方法。方法:将含骨修复材料的腰椎椎体骨组织标本进行分割暴露组织切面,梯度浓度乙醇脱水后经 Technovit 7200 VLC 光聚树脂浸润,经黄蓝光共同辐照进行光聚合包埋,借助硬组织病理切磨系统制备含骨修复材料不脱钙病理组织切片。结果:结果显示通过上述方法制备的病理组织切片,经苏木精 - 伊红(HE)染色及甲苯胺蓝染色后光学显微镜下观察能较好地显示骨的各种组织细胞结构,可清晰的观察到骨小梁的走向及连接情况。结论:研究建立了含骨修复材料骨组织标本病理组织切片制备方法,实现了含骨修复材料不脱钙骨组织病理切
片的制备,经病理染色后实现了带植入物的组织学观察,为生物材料及医疗器械动物试验研究提供了新的病理检测手段及组织学评价途径。
关键词:小型猪腰椎椎体;含骨修复材料骨组织标本;树脂包埋法;不脱钙病理组织切片制备
中图分类号:R-33;R318.08 文献标识码:A 文章编号:1673-6273(2023)06-1017-05
【前言】
用于骨修复的生物材料及器械在进行临床试验前均需要进行临床前安全性和有效性动物试验研究,以预测其应用于临 床可能发生的不良作用[1,2]。骨修复材料的动物试验研究需要制备合适的骨缺损动物模型,将骨修复材料植入到制备的骨缺损区域,评价骨缺损部位的局部炎症反应、骨整合程度、骨重建情况,对该骨修复材料的安全性及有效性进行评价[3,4] 。生物材料及医疗器械动物试验周期结束后,需要剖检、取样,切取连带植入物及其周边骨组织进行病理组织切片制备,以观察生物材料及医疗器械与宿主骨组织结合界面的结合情况及其在动物体内的吸收降解情况 。与普通的石蜡包埋组织切片制备方法相比,埋置有植入物的骨组织标本进行组织切片制备时采用树脂包埋病理组织切片制备方法不需要进行脱钙处理,不需要额外剔除组织内埋置的植入物,可完整的观察到植入物与宿主骨组织结合界面的组织反应情况,实现对植入物与骨组织结合界面组织细胞学变化的研究。本研究对植入了骨修复材料小型猪腰椎椎体不脱钙病理组织切片制备方法进行了研究,以期能为相 关研究人员提供参考。
01材料与方法
1.1 材料1.1.1 组织标本 按照《医疗器械动物试验研究注册审查指导 原则 第二部分:试验设计、实施质量保证(2021 年第 75 号)》进行骨修复材料产品安全性和有效性评价动物试验研究方案的设计与实施[5]。试验研究制备小型猪腰椎椎体骨缺损动物模型, 将委托方提供的骨修复材料植入到制备的缺损部位,动物试验研究周期结束后获得了植入了骨修复材料的腰椎椎体骨组织标本。1.1.2 主要试剂及仪器设备 主要试剂:10 %中性福尔马林溶 液(购自济南百博生物技术股份有限公司),无水乙醇(购自国药集团化学试剂有限公司),苏木精染液、伊红染液及甲苯胺蓝染色试剂盒(购自北京索莱宝科技有限公司),Technovit 7200 光聚树脂(购自德国 EXAKT 公司)。主要仪器设备:E300CP 型 硬组织切片机、E400CS 型 硬组织磨片机、E402 型 平行粘片装置、E510 型脱水浸润仪、E520 型光固化包埋机、 E530 型 干燥渗透聚合装置、E312 型 骨组织病理切割机(德国 EXAKT 公司)。1.2 方法1.2.1 组织标本的固定将切取下的小型猪椎体骨组织标本 放入 10 %中性福尔马林溶液中进行固定,固定 24 h 后,更换新 的 10 %中性福尔马林溶液,进一步继续固定,固定时间不少于 1 周。1.2.2 组织标本的切割取材 将充分固定后的骨组织标本借 助 E312 型骨组织病理切割机切割为约 7 mm 厚度的标本,置 于 10 %中性福尔马林溶液中继续固定至少 12 h ,流水冲洗至 少 1 h,以水置换出组织中渗透的固定液。1.2.3 组织标本的脱水及浸润 在抽真空条件下将固定充分经流水冲洗后的骨组织标本逐级浸入梯度乙醇进行脱水处理, 脱水程序见表 1 。在抽真空条件下将脱水完全的骨组织标本逐 级浸入不同体积比的 Technovit 7200VLC 树脂 / 乙醇混合液中 进行浸润处理,浸润程序见表 2。


1.2.4 组织标本的光固化包埋聚合 取出浸润完全的骨组织标本置入光固化包埋专用的模具中,加入光聚树脂,借助 EX- AKT 530 干燥渗透聚合装置进行抽真空处理,排净包埋模具内 残存的气泡后进行固化聚合操作。固化过程由低强度的黄光与高强度的蓝光共同辐照完成 ,先黄光辐照 6 h 后蓝光辐照 8 h 完成骨组织标本的光固化聚合。含骨修复材料的腰椎椎体骨组织标本光固化包埋标本块,见图 1。
1.2.5 组织标本的平行粘片制作将聚合过的组织标本树脂 包埋块从包埋模具中取出 ,利用 Technovit4000 粘合剂套装将 包埋有骨组织的树脂包埋块黏于载玻片上。经 EXAKT 300 CP 硬组织切片机切割 ,暴露出需要的组织切面 ,利用 EXAKT 400CS 硬组织磨片机对切面进行抛光处理 ,另取一张载玻片, 在 EXAKT 402 载片黏合装置上用 Technovit 7210VLC 精密粘合剂将该载玻片黏附于标本块的抛光面,组织标本的平行粘片即制作完成。
1.2.6 组织标本的切片及磨片 经 EXAKT 300CP 硬组织切 片机将包埋有组织标本的树脂块进行切割,一般将切割厚度设 为 200-300 μm,切片完成后,取下切片,经 EXAKT 400CS 硬组 织磨片机进行磨片操作,磨片过程中要用到不同规格的研磨纸和抛光纸,先进行粗磨,再进行精磨,最后进行抛光处理,将组织磨至 20 μm 左右 。含骨修复材料的腰椎椎体骨组织标本切磨片,见图 2。

1.2.7 含骨修复材料组织切片的染色将制备的含骨修复材 料的组织切磨片经蒸馏水充分清洗后,进行病理染色 。含骨修复材料腰椎椎体骨组织病理切片 HE 染色方法:苏木精染液 30 min,自来水充分冲洗,1 %盐酸乙醇分化 30 s,流水冲洗后再入温水返蓝,置伊红染色液 5 min,自来水冲洗,待组织切片自然干燥后经 Technovit 7200VLC 封片后,置光学显微镜下镜检观察。含骨修复材料腰椎椎体骨组织病理切磨片甲苯胺蓝染色方 法:将制备的骨组织标本病理切磨片置于体积分数 1 %甲苯胺 蓝染液中 20 min 后,自来水充分冲洗,待组织切片自然干燥后 经 Technovit 7200VLC 封片后,置光学显微镜下镜检观察。02 结果
2.1 制备的含骨修复材料小型猪腰椎椎体不脱钙骨组织病理切片 HE 染色结果通过上述方法制备了含骨修复材料小型猪腰椎椎体不脱钙骨组织病理切片,经 HE 染色后,光学显微镜下观察可见试验研究植入的骨修复材料,呈浅灰色 。组织切片经 HE 染色后 细胞核呈蓝色,胞质呈红色,胞核、胞质着色对比鲜明,骨组织细胞未见移位变形,可清晰辨认骨的各种细胞成份,实现了含植入物不脱钙骨组织的组织细胞学观察,见图 3。

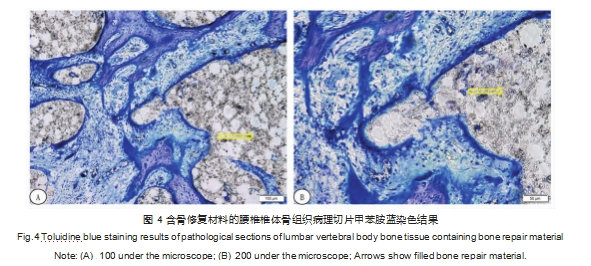
2.2 制备的含骨修复材料小型猪腰椎椎体不脱钙骨组织病理切片甲苯胺蓝染色结果含骨修复材料小型猪腰椎椎体不脱钙骨组织病理切片经 甲苯胺蓝染色后,光学显微镜下观察可见试验研究植入的骨修复材料,呈浅灰色 。组织细胞经甲苯胺蓝染色后,能较好地显示骨的各种组织细胞结构 ,可清晰的观察到骨小梁的走向及连接情况,可以观察到植入的骨修复材料与宿主骨结合情况, 见图 4。
03 讨论
骨组织标本采用石蜡包埋法进行病理切片制作时,必须先用乙二胺四乙酸二钠(EDTA)、硝酸、甲酸等脱钙液对骨组织标本进行脱钙处理[6-8]。在骨组织内埋置有植入物的情况下石蜡包埋组织切片并不适用 ,原因是硬化后的石蜡虽具有一定的硬度,但其硬度不足以支撑去切组织内包埋的植入物,切片过程会造成蜡块碎裂[9-11]。
树脂包埋法制备病理组织切片与常规 " 石蜡包埋组织切 片 " 相比,制片步骤更为复杂繁琐,制片周期更长,组织标本需 要历经组织切割暴露切面、梯度乙醇脱水、不同体积比的 Tech- novit 7200VLC 树脂 / 乙醇混合液浸润、光聚合包埋、制备平行 粘片,切片、磨片,才可制备出一张不脱钙的骨组织病理切片。上述报道的骨组织病理切片制备方法所适用的病理染色方法 少,这是其缺陷所在,造就了适用范围受限 。同时,这种方法制 备病理切片周期长 ,仅组织标本的浸润处理过程就需要近 40 天 。其优点是骨组织制片过程中不需要脱钙处理,组织在埋置 有植入物的情况下,不需要剔除植入物,这是 " 石蜡包埋组织 切片 " 所实现不了的,上述报道的骨组织病理切片制备方法可 作为传统的 、经典的 " 石蜡包埋组织切片技术方法 " 的补充。利用该技术方法制备含骨修复材料腰椎椎体不脱钙病理组织切片时,需注意以下细节:(1)若切取的骨组织标本体积较大, 应延长固定时间且固定过程中,应多次更换新的固定液,骨组织标本经骨组织病理切割机分切后 ,应该继续固定至少 12 h, 以使组织标本得到充分的固定 。(2)因不脱钙的骨组织标本致 密紧实 ,应在抽真空负压的条件下进行骨组织标本的脱水、浸润处理,以使组织标本脱水充分,树脂包埋液浸润更加完全,更利于后续的组织切片制备。(3)进行光聚合固化包埋时,应先利 用干燥渗透聚合装置抽真空 ,排净包埋模具内残存的气泡,以 免影响组织块的聚合、固化。(4)平行粘片制作过程中应利用磨 片机充分对需要观察的组织切面抛光处理,以免出现组织切片 厚薄不一现象 。(5)在磨片时,磨盘转速应设置的尽可能的低, 以免造成植入的骨修复材料与宿主骨组织脱离,致使长入骨修 复材料的新生骨组织丢失,影响后期的组织病理学分析。
与普通的石蜡包埋法病理组织切片制备方法不同,本研究 采用 Technovit 7200 VLC 光聚树脂进行骨组织标本光固化包埋,借助 EXAKT 硬组织病理切磨系统制备骨组织标本的不脱 钙病理组织切片,组织切片制备过程中所用的并不是传统的病 理切片刀,而是镶嵌有金刚石的无齿切割带锯,以 " 锯 " 的形式对组织进行切割,制备组织切片 。该方法制备的病理切片最 显著的特点是不需要对骨组织进行脱钙处理,可使骨组织结构 形态保持完好,骨的矿化结构不被破坏,可用于含金属、陶瓷、 骨水泥等骨修复材料的临床前安全性和有效性的骨缺损修复 动物试验研究[12] 。同时,该技术方法制片过程中不需要剔除植 入到骨组织中的植入物,保持了骨组织与植入物之间原有的组 织结构形态,可直观反应结合界面的组织生长结合情况,这对 骨缺损修复试验的组织长入研究具有重要意义,可用于 3D 打 印多孔洞类材料组织长入等生物组织相容性研究[13]。
生物材料及医疗器械动物试验研究的目的是预测其应用 于临床可能发生的不良反应,是医疗器械临床前安全性评价必须进行的一项试验研究[14]。动物试验研究组织病理学评价是该评价体系中重要的一环,用以确定产品组织相容性,是评价其安全性并判定是否可以应用于临床的重要研究手段[15,16] 。树脂包埋法制备病理组织切片无需进行脱钙处理,在动物试验研究中结合动物活体亲骨荧光素标记技术,可实现动态测量骨修复过程中的新生骨矿化率和矿化速率 ,进行骨形态计量学研究[17,18] 。制备的病理组织切片最显著的特点是不破坏植入到骨组织中的植入物,保持了骨组织与植入物之间原有的组织结构 形态,该技术方法结合扫描电镜技术,可实现观察成骨细胞在骨修复材料表面及孔隙内附着及生长情况,从而判断骨修复程 度,同时结合扫描电镜技术可实现观察骨修复材料表面侵蚀及 骨质沉积情况的研究[19-22]。
20 世纪 80 年代,为研究骨组织的矿化程度及新骨形成情 况,塑料包埋技术开始应用于骨组织病理切片的制备,近年来许多实验室在塑料包埋方法上进行了创新,特别是在包埋聚合 液及其聚合条件方面做了多种改进[23-26] 。有文献报道用甲基丙 烯酸甲酯(MMA)及邻苯二甲酸二丁酯(DBP)为渗透剂,甲基丙烯酸甲酯为包埋剂,包埋聚合制备骨组织塑料包埋切片的技术方法,但这一制片技术因操作烦琐,制作周期长,且塑料包埋 块制备过程复杂,组织切片制备过程对温度要求高,目前该技术方法仍然在用,但未得到广泛应用[27,28]。本研究制备不脱钙骨组织病理切片包埋剂采用的是光聚树脂,通过黄光与蓝光共同辐照完成组织包埋块的包埋聚合 ,与传统的 " 石蜡包埋组织切片 " 方法及 " 塑料包埋技术 " 组织切片方法制备骨组织病 理切片所用的包埋剂不同 ,组织标本的浸润处理及切片方式 也不同。
本研究制备的含骨修复材料腰椎椎体不脱钙病理组织切片,光学显微镜下可清晰观察骨缺损部位植入骨修复材料后组 织结合界面骨的各种组织细胞结构,可进行骨缺损修复后骨组 织重建进程及炎症反应研究,适用于生物材料及医疗器械临床前动物试验安全性评价的组织病理学研究。
技术服务咨询 步经理 18910422384
 官方微信
官方微信艾佧科技(北京)有限公司 地址:北京市经济技术开发区地盛南街1号1幢3041室
2020@ 艾佧科技(北京)有限公司 京ICP备10236589号